DaS EDC
- 按照GAMP5 系统验证,系统安全可靠;
- 符合 FDA21 CFR Part11电子签名要求;
- 符合 ICH GCP 、NMPA等法规规范;
- 灵活的数据库结构,满足不同临床试验要求;
- 多语言版本,支持全球多中心临床研究开展;
- 使用国内高标准IDC机房,异地备份,保证数据安全;
- 强大技术团队开发系统;运维工程师 7×24h 快速响应,提供专业技术支撑。


高效、操作简便
超人性化界面UI布局、功能设计,各模块能够快速精准切换,减少用户使用成本,提高效率;
数据标准、分析
提供标准化数据报表,轻松提供管理团队数据不同维度管理;支持CDISC标准ODM.xml导入导出。
操作方式多样
支持研究中心、受试者、访视期、表单、字段从大到小各级别单点操作机批量完成任务,减少重复系统操作;
平台化管理
平台集成管理模块进行研究创建、研究中心管理、编码配置、数据共享设置;
翻译工作台
支持配置、数据翻译,提供数据翻译全解决方案;
并可自主选择在线翻译、离线翻译;翻译审校流程保证数据准确性
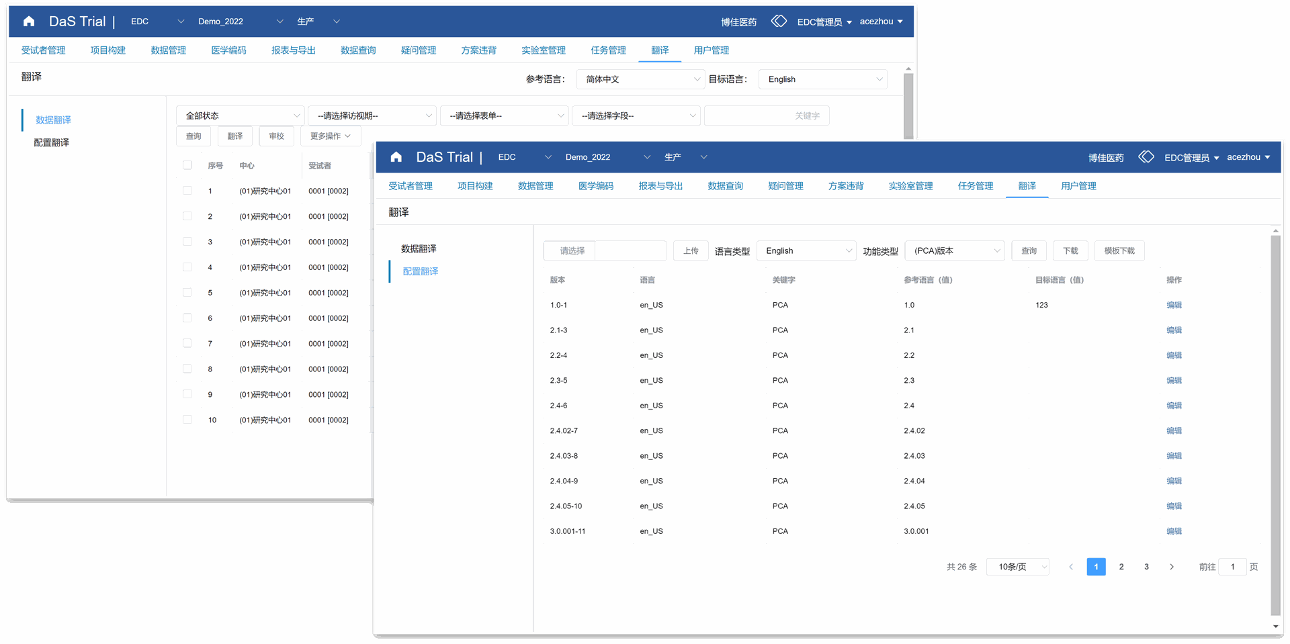
数据标准化
支持CIDSC标准的ODM.xml导入导出;
系统API进行不同供应商系统的数据交换;包括Subject data和Admin data,根据Admin Data进行数据库配置读取更新;

丰富的应用经验
- 累计超过 3000 多项临床试验使用DaS EDC进行数据采集、管理,涵盖Ⅰ~ Ⅳ 期新药注册和国家级科研项目,应用于各个适应症。
- 采集超过 50 万例受试者,应用于多项国家级重大专项研究,如艾滋病防治、HPV大数据库;支持上海市三年行动计划数据库平台。
- DaS EDC已在800余家医院/机构使用,应用覆盖全国(含香港、台湾地区)。
- 服务 600 余家企业与科研单位,亦参与国际多中心试验,经验丰富。